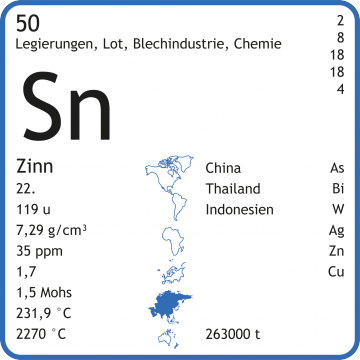
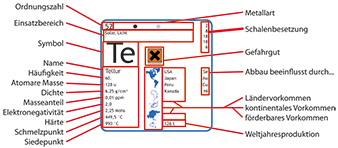
Zinn-Chemie » Eigenschaften
Zinn kann drei Modifikationen mit verschiedener Kristallstruktur und Dichte annehmen:
- α-Zinn (kubisches Diamantgitter, 5,75 g/cm3) ist unterhalb von 13,2 °C stabil und besitzt einen Bandabstand von EG = 0,1 eV. Damit wird es je nach Interpretation als Halbmetall oder Halbleiter eingeordnet. Seine Farbe ist grau.
- β-Zinn (verzerrt oktaedrisch, 7,31 g/cm3) bis 162 °C, Oberfläche silberweiß.
- γ-Zinn (rhombisches Gitter, 6,54 g/cm3) oberhalb von 162 °C oder unter hohem Druck.
Daneben kann noch eine zweidimensionale Modifikation namens Stanen (ähnlich der Kohlenstoffmodifikation Graphen) synthetisiert werden.
Natürliches Zinn besteht aus zehn verschiedenen stabilen Isotopen; das ist die größte Anzahl unter allen Elementen. Außerdem sind noch 28 radioaktive Isotope bekannt.
Die Rekristallisation von β-Zinn zu α-Zinn bei niedrigen Temperaturen äußert sich als die sogenannte Zinnpest.
Beim Verbiegen des relativ weichen Zinns, beispielsweise von Zinnstangen, tritt ein charakteristisches Geräusch, das Zinngeschrei (auch Zinnschrei), auf. Es entsteht durch die Reibung der β-Kristallite aneinander. Das Geräusch tritt jedoch nur bei reinem Zinn auf. Bereits niedrig legiertes Zinn zeigt diese Eigenschaft nicht; z. B. verhindern geringe Beimengungen von Blei oder auch Antimon das Zinngeschrei. Das β-Zinn hat einen abgeflachten Tetraeder als Raumzellenstruktur, aus dem sich zusätzlich zwei Verbindungen ausbilden.
Durch die Oxidschicht, mit der Zinn sich überzieht, ist es sehr beständig. Von konzentrierten Säuren und Basen wird es allerdings unter Entwicklung von Wasserstoffgas zersetzt. Jedoch ist Zinn(IV)-oxid ähnlich inert wie Titan(IV)-oxid. Zinn wird von unedleren Metallen (z. B. Zink) reduziert; dabei scheidet sich elementares Zinn schwammig oder am Zink haftend ab.